O ar é uma matéria que possui propriedade de ocupar todo o espaço do ambiente em que não exista qualquer outra matéria, ao mesmo tempo apresenta uma compressibilidade, pois tende a diminuir de volume quando sofre a ação se ser comprimido. O que faz com que o ar mantenha essas características são os diferentes elementos como vapor d’água, microrganismos e também os gases componentes de sua formação – oxigênio, gases nobres, nitrogênio e gás carbônico.
Dentre esse gases constituintes do ar, um possui grande destaque, o oxigênio, responsável pela respiração. O que caracteriza o homem, as plantas e os animais como seres vivos aeróbicos. Além dessa importância, o gás também é capaz de atuar na “queima” de alimentos, produzindo a energia adequada para que os órgãos mantenham sua atividade e funcionem corretamente.

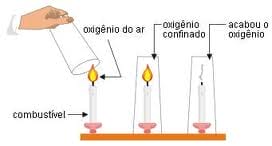
O oxigênio também serve como gás comburente, ou seja, alimenta a combustão, uma reação química que sempre produz calor mas em forma de energia com a associação de um combustível, seja sólido, gasoso ou líquido. Um exemplo é a chama da vela que acesa produz energia luminosa e térmica, ou seja, luz e calor. Outra substância combustível é a gasolina que ao sofre uma combustão, queima no motor do carro gerando duas energias – mecânica e térmica, fazendo com que ele se mova.
Quando ocorre a combustão, é possível presenciar a liberação de gás carbônico e vapor d’água, outros gases ainda podem causar danos a atmosfera por serem poluentes. Dentre os combustíveis fósseis, que mais causam prejuízo ao meio ambiente são os derivados de petróleo e o carvão, mais comumente usados em fábricas e veículos.
Uma combustão representa as seguinte ação:
- A reação química que sempre produz calor – combustão
- Substância que pode ser queimada – combustível Ex:(vela)
- O alimento da combustão – comburente Ex: (gás oxigênio)
A combustão é essencial para inúmeras utilidades humanas, dentre a s ais comuns estão o eventos que ocorrem no fogão a gás, combustível de carros, aviões, nas indústrias, e até mesmo em uma atividade de siderúrgico quando está realizando uma solda utilizando um maçarico.
Da mesma forma que contribui, a combustão também pode causar agravantes tanto para o homem quanto para o meio ambiente. São os resíduos tóxicos provenientes da queima que geram a poluição da atmosfera. Se o O2(oxigênio) entrar em contato com o Fe(ferro) pode provocar a ferrugem, destruindo máquinas, carros, entre outros.


